生物相容3D打印材料介紹
魔猴君 知識堂 201天前
用于人體的3D打印產品應由不會引起過敏或毒性反應的生物相容性材料制成。但就3D打印材料而言,生物相容性是什么意思?哪些材料具有生物相容性?
如今,可用于3D打印的生物相容性材料選項比以往任何時候都多,這使得牙科和醫療專業人士以及各種制造商能夠3D打印用于短期或長期皮膚接觸(可穿戴設備、COVID測試拭子、矯形器、耳塞、個人防護設備)或用于人體內部(假牙、關節置換、骨植入物、血管支架)的產品。甚至醫療器械開發公司也使用生物相容性材料來3D打印其產品原型。
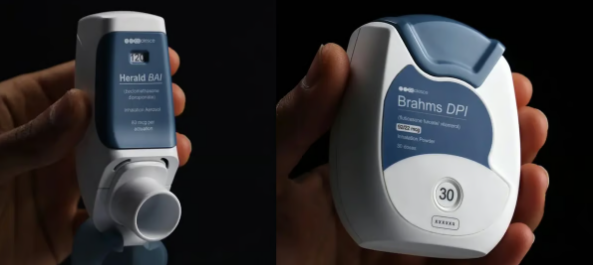
這些3D打印吸入器原型由諾華旗下的英國分部Coalesce Product Development使用Formlabs 3D打印機和生物相容性樹脂制成,將其吸入器產品的交貨時間縮短了80%以上(來源:Formlabs)
讓我們通過研究兩個關鍵應用領域來探索生物相容性3D打印材料的多種類型和用途,這兩個領域可以作為無數其他應用的模型:牙科和假肢。稍后我們將討論永久性身體植入物(如膝關節置換和顱骨植入物)是用什么材料3D打印出來的。
當然,本篇生物相容性材料概述并非旨在提供任何形式的醫療指導,請記住,美國、歐盟、亞洲和印度的生物相容性法規各不相同。
生物相容性牙科材料
Asiga牙科樹脂(來源:Asiga)
整個牙科行業已迅速將3D打印應用于一系列產品。從模型到臨時假牙再到永久植入物,3D打印使用塑料和金屬,以消費者期望的速度和價格提供牙醫所需的患者專用產品。事實上,根據Zion Market Research的數據,2021年全球牙科3D打印市場價值約為32.5億美元。
牙醫通常使用樹脂3D打印(也稱為立體光刻)來生產假牙、護齒器、手術工具以及許多其他產品,這些產品會暫時或永久地放入口中。市面上有各種各樣的樹脂,在生物相容性方面,制造商擁有特定的分類、評估和行業標準,這些標準看起來像是秘密代碼。讓我們來看看這些標簽和數字的真正含義。
生物相容性的3D打印材料類別
根據FDA的規定,美國將生物相容性分為I類、II類或III類(根據MDCG的規定,歐盟則將其分為I類、II類或III類)。世界其他地方也有類似的系統,但分類不同。例如,由于沒有國際標準,美國的II類產品在中國可能屬于III類。在本文中,我們將重點介紹美國和歐盟標準。
盡管您會看到以I類形式銷售的樹脂,但材料本身并未歸類,而是需要提交使用該材料制成的產品進行測試(如果需要測試)。
I類醫療器械屬于低風險至中等風險,需要一般控制。幾乎一半的醫療器械被視為I類,95%的醫療器械不受任何監管監督。I類醫療器械的一般示例包括彈性繃帶和手持式手術器械,它們僅接觸完整的皮膚。在牙科3D打印方面,I類材料通常用于制作牙科印模的試戴設備。
II類醫療器械具有中等至高風險,需要特殊控制。這些材料一旦制造商在FDA注冊并列出,并符合適用要求,即可在美國銷售。II類器械的類型包括可拆卸皮膚釘和牙科中的永久性修復體、嵌體、覆蓋體和假牙。這些產品指定用于與血液、體液、器官、組織和細胞接觸。
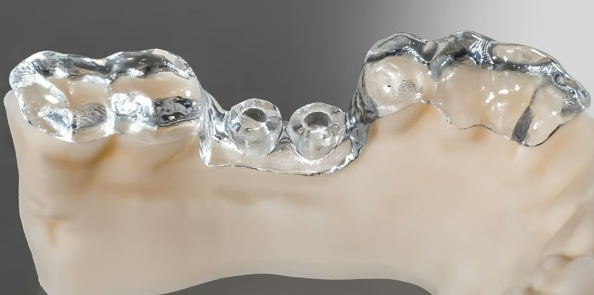
采用Detax的Freeprint Ortho樹脂制作的牙科手術導板(來源:Detax)
根據暴露時間,這兩個類別進一步細分為子類別(a、b和c),從有限時間到長時間再到永久時間。例如,II類a表示II類設備使用時間有限,具體來說,使用時間少于24小時。子類別“b”表示長時間使用(24小時至30天),子類別“c”表示永久使用(超過30天)。
生物相容性不僅僅是一種衡量標準,而是國際標準化組織(ISO)規定的多種衡量標準。具體來說,標準10993及其子類別表示生物相容性的類型。例如,ISO標準10993-5是對材料對活細胞有毒(或細胞毒性)的風險的評估,而10993-10則涉及材料作為刺激物或致敏劑的風險。還有對材料是否能夠誘發基因突變、引起皮疹或引起廣泛毒性的評估。您的3D打印材料可能符合部分或全部標準。
等級劃分基于設備的風險,而ISO 10993則基于與身體組織和體液的接觸時間和接觸類型,這在選擇設備材料時是最重要的因素。
制造商會披露材料在評估和測試后是否符合生物相容性國際標準要求。制造商通常甚至會披露進行測試的實驗室。
ISO還有其他標準值得參考。ISO 22112涉及用聚合物或陶瓷制成的(包括3D打印的)假牙的材料特性。對于聚合物基牙冠和貼面材料,有ISO 10477;對于假牙基托聚合物,有ISO 20795。請注意,這些標準并非3D打印所獨有,也適用于模制和加工牙科產品所用的材料。
讓我們以一種生物相容性3D打印樹脂為例。3D打印機和材料制造商Formlabs的假牙樹脂附帶一份數據表,上面說該材料已在明尼蘇達州圣保羅的藥明康德實驗室進行了醫療器械生物學評估測試,并根據ISO 10993認證為生物相容性,無致突變性、無細胞毒性,不會引起紅斑或水腫反應,不是致敏劑,也不會引起全身毒性。用這種材料制成的部件的后固化性能符合ISO 22112和ISO 10477。目前,Formlabs的16種材料已根據各種ISO 10993、ISO 18562和USP Class VI端點公開測試,結果已發布在公司網站上。
您用于3D打印的材料應該能夠提供Formlabs在技術數據表中或通過聯系制造商所提供的特定級別。
您可能在材料上看到的另一個標識是USP VI級,它指的是美國藥典(USP)的一組生物相容性測試要求,該組織是一個非營利組織,其標準為美國食品藥品管理局(FDA)的決策提供參考。這種測試是確定材料生物相容性的最常用方法之一。共有六個等級,其中VI級最為嚴格,旨在證明塑料材料中滲出的化學物質不會引起有害反應或長期身體影響。
在材料上看到一些實際上毫無意義的術語并不罕見。例如,“FDA 510(k)批準”或“FDA 510(k)批準”實際上并不是認證。當FDA通過510(k)批準一種設備時,它不會檢查該產品對患者使用是否安全或有效。它只是同意制造商的說法,即該設備(或材料)與市場上已有的其他設備相似。“CE認證”也是如此。歐盟產品上的CE字母意味著制造商證明該產品符合歐洲健康、安全和環境保護標準。它不是質量指標或認證標志。

編譯整理:ALL3DP